ワクチンと健康会議では専門家らが「人類に無限の思考をもたらすmRNAワクチンに誰もが注目すべきだ」と呼び掛けた。では、mRNAワクチンとは一体何なのでしょうか?それはどのように発見され、その応用価値は何ですか?世界中で猛威を振るう新型コロナウイルス感染症に対抗できるだろうか?私の国はmRNAワクチンの開発に成功しましたか?今日は、mRNAワクチンの過去と現在について学びましょう。
01
mRNAワクチンのmRNAとは何ですか?
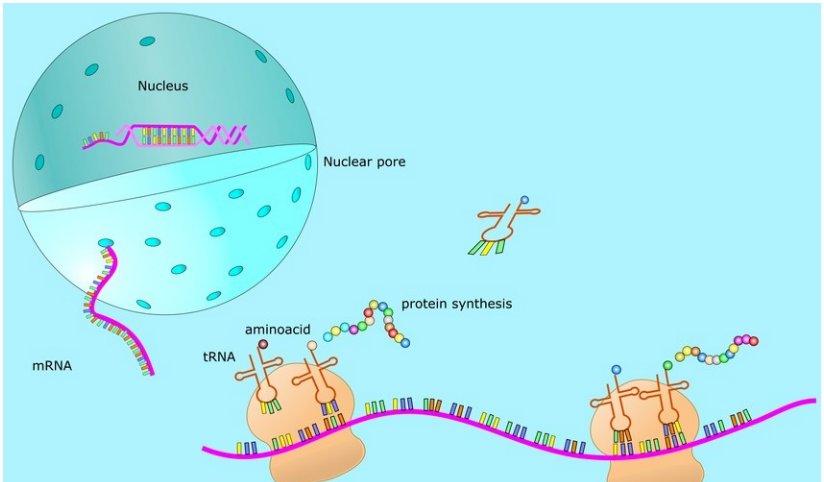
mRNA(メッセンジャーRNA)、つまりメッセンジャーRNAは、DNA鎖から鋳型として転写される一本鎖RNAの一種で、タンパク質の合成を導く遺伝情報を担っています。平たく言えば、mRNAは二本鎖DNAの一本鎖の遺伝情報を核内で複製し、核を出て細胞質内でタンパク質を生成します。細胞質では、リボソームがmRNAに沿って移動し、その塩基配列を読み取って対応するアミノ酸に翻訳し、最終的にタンパク質を形成します(図1)。
図1 mRNAの作業プロセス
02
mRNA ワクチンとは何ですか?またその特徴は何ですか?
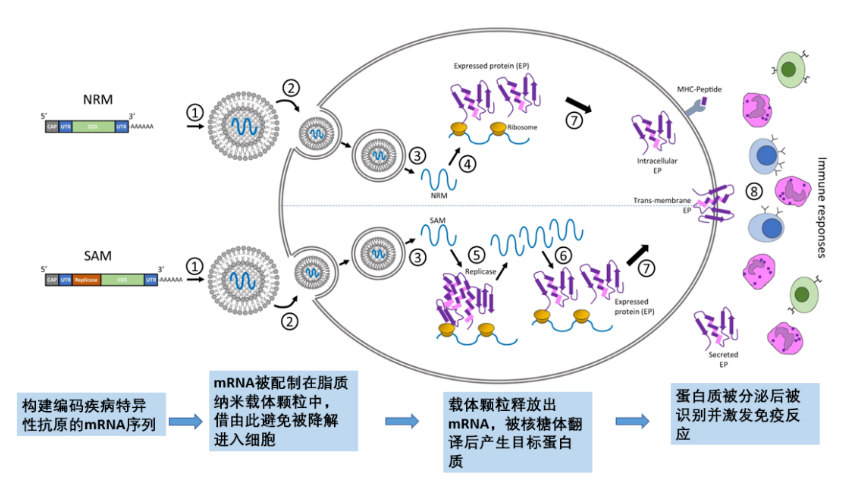
mRNA ワクチンは、疾患特異的抗原をコードする mRNA を体内に導入し、宿主細胞のタンパク質合成機構を利用して抗原を生成し、それによって免疫応答を引き起こします。通常、特定の抗原のmRNA配列は、さまざまな疾患に応じて構築され、パッケージングされ、新規の脂質ナノキャリア粒子によって細胞内に輸送されます。その後、ヒトリボソームのmRNA配列を使用してmRNA配列が翻訳され、疾患抗原タンパク質が生成されます。このタンパク質は、分泌後に自己免疫系によって認識されて免疫応答を生成し、疾患予防の役割を果たします(図2)。
では、このタイプの mRNA ワクチンは従来のワクチンと比べて何がユニークなのでしょうか?mRNA ワクチンは最先端の第 3 世代ワクチンであり、その安定性の向上、免疫原性の調節、新しい送達技術の開発にはさらなる研究が必要です。
従来のワクチンの第 1 世代には、主に不活化ワクチンと弱毒化生ワクチンが含まれており、これらが最も広く使用されています。不活化ワクチンとは、まずウイルスや細菌を培養し、次に熱や化学薬品(通常はホルマリン)で不活化することを指します。弱毒生ワクチンとは、さまざまな処理後に突然変異して毒性を弱める病原体を指します。しかし、免疫原性はまだ保持されています。体内に接種しても病気は発生しませんが、病原体は体内で成長して増殖し、体の免疫反応を引き起こし、長期または生涯にわたる防御を獲得する役割を果たす可能性があります。
第 2 世代の新しいワクチンには、サブユニット ワクチンと組換えタンパク質ワクチンが含まれます。サブユニットワクチンは、病原菌の主要な防御免疫原成分で作られたワクチンサブユニットワクチンです。つまり、化学的分解または制御されたタンパク質分解を通じて、細菌やウイルスの特殊なタンパク質構造が抽出され、選別されます。免疫学的に活性な断片で作られたワクチン。組換えタンパク質ワクチンは、異なる細胞発現系で生成される抗原組換えタンパク質です。
第 3 世代の最先端ワクチンには、DNA ワクチンと mRNA ワクチンが含まれます。特定の抗原タンパク質をコードするウイルス遺伝子断片(DNAまたはRNA)を動物の体細胞に直接導入(人体へのワクチン注射)し、宿主細胞のタンパク質合成系を介して抗原タンパク質を産生させ、宿主に抗原タンパク質応答に対する免疫の産生を誘導し、疾患の予防と治療の目的を達成することです。両者の違いは、DNA が最初に mRNA に転写されてからタンパク質が合成されるのに対し、mRNA は直接合成されることです。
03
mRNAワクチンの発見の歴史と応用価値
mRNA ワクチンに関して言えば、mRNA ワクチンの出現のための強固な科学研究基盤を築いた傑出した女性科学者、カティ・カリコについて言及する必要があります。彼女は在学中、mRNA に対する研究に興味を持っていました。40年以上の科学研究キャリアの中で、彼女は度重なる挫折に見舞われ、科学研究費の申請もせず、安定した科学研究の地位も得られなかったが、彼女は常にmRNA研究を主張し続けた。
mRNA ワクチンの出現には 3 つの重要なノードがあります。
最初のステップでは、細胞培養によって目的の mRNA 分子を生成することに成功しましたが、mRNA を体内で機能させる際に問題が発生しました。mRNA をマウスに注射すると、マウスの免疫系によって飲み込まれてしまうのです。それから彼女はワイズマンに会いました。彼らは、mRNA が免疫反応を回避するために、tRNA 内のプソイドウリジンと呼ばれる分子を使用しました。][2]。
第 2 段階では、2000 年頃、Pieter Cullis 教授は、遺伝子サイレンシング用途のための siRNA の in vivo 送達のための脂質ナノテクノロジー LNP を研究しました [3][4]。ワイズマン組織カリコら。らは、LNP が in vivo での mRNA の適切なキャリアであり、治療用タンパク質をコードする mRNA を送達するための貴重なツールになる可能性があることを発見し、その後、ジカウイルス、HIV、腫瘍の予防において検証されました [5] ] [6] [7] [8]。
第 3 段階では、2010 年と 2013 年に、Moderna と BioNTech がさらなる開発のためにペンシルバニア大学から mRNA 合成に関する特許ライセンスを相次いで取得しました。カタリン氏は、mRNAワクチンの開発をさらに進めるため、2013年にBioNTechの上級副社長にも就任した。
現在、mRNA ワクチンは感染症、腫瘍、喘息に使用できます。世界中で猛威を振るう新型コロナウイルス感染症の場合、mRNAワクチンがその先兵としての役割を果たす可能性がある。
04
新型コロナウイルス感染症におけるmRNAワクチンの応用見通し
新型コロナウイルス感染症(COVID-19)の世界的流行を受けて、各国は流行を抑制するワクチンの開発に懸命に取り組んでいる。新しいタイプのワクチンとして、mRNA ワクチンは新たな感染症の流行の到来において主導的な役割を果たしています。多くのトップジャーナルが、SARS-CoV-2 新型コロナウイルスにおける mRNA の役割を報告しています (図 3)。
図3 新型コロナウイルスを予防するmRNAワクチンに関する報告書(NCBIより)
まず、多くの科学者がマウスを使った新型コロナウイルスに対するmRNAワクチン(SARS-CoV-2 mRNA)の研究を報告している。たとえば、脂質ナノ粒子でカプセル化されたヌクレオシド修飾 mRNA (mRNA-LNP) ワクチンは、単回投与で強力な 1 型 CD4+ T および CD8+ T 細胞応答、長命の血漿およびメモリー B 細胞応答、および強力で持続的な中和抗体応答を誘導します。これは、mRNA-LNP ワクチンが COVID-19 に対する有望な候補であることを示しています[9][10]。
第二に、一部の科学者は、SARS-CoV-2 mRNA と従来のワクチンの効果を比較しました。組換えタンパク質ワクチンとの比較: mRNA ワクチンは、胚中心反応、Tfh 活性化、中和抗体産生、特異的メモリー B 細胞、および長寿命形質細胞の点でタンパク質ワクチンよりもはるかに優れています [11] 。
その後、SARS-CoV-2 mRNA ワクチン候補が臨床試験に入ると、ワクチンの防御期間が短いことについて懸念が生じました。科学者らは、mRNA-RBDと呼ばれるヌクレオシド修飾mRNAワクチンの脂質カプセル化型を開発した。1回の注射で強力な中和抗体と細胞反応を生成することができ、2019-nCoVに感染したモデルマウスをほぼ完全に防御することができ、高レベルの中和抗体が少なくとも6.5か月間維持されます。これらのデータは、mRNA-RBD の単回投与が SARS-CoV-2 感染に対する長期的な防御を提供することを示唆しています [12]。
BNT162b ワクチンなど、新型コロナウイルス感染症に対する安全で効果的な新しいワクチンの開発に取り組んでいる科学者もいます。マカクザルをSARS-CoV-2から保護し、下気道をウイルスRNAから保護し、非常に強力な抗体を産生し、疾患が悪化する兆候は見られませんでした。現在、2 つの候補品が第 I 相試験で評価中であり、国際的な第 II/III 相試験でも評価が進行中であり、申請が目前に迫っています [13]。
05
世界のmRNAワクチンの状況
現在、BioNTech、Moderna、CureVac は、mRNA 治療の世界トップ 3 リーダーとして知られています。その中で、BioNTechとModernaは新しいクラウンワクチンの研究開発の最前線に立っています。モデルナはmRNA関連の医薬品やワクチンの研究開発に注力してきた。新型コロナウイルス感染症(COVID-19)第III相試験ワクチンmRNA-1273は、同社で最も急速に成長しているプロジェクトである。BioNTech は、世界をリードする mRNA 医薬品およびワクチンの研究開発会社でもあり、合計 19 の mRNA 医薬品/ワクチンを保有しており、そのうち 7 つは臨床段階に入っています。キュアバックはmRNA医薬品・ワクチンの研究開発に注力しており、腫瘍、感染症、希少疾患を中心にGMP準拠のRNA生産ラインを確立した世界初の企業です。
関連製品:RNase阻害剤
キーワード: miRNA ワクチン、RNA 分離、RNA 抽出、RNase 阻害剤
参考文献: 1.K カリコ、バックスタイン M 、Ni H 他Toll 様受容体による RNA 認識の抑制: ヌクレオシド修飾の影響と RNA の進化的起源 [J]。免疫、2005、23(2):165-175。
2. K カリコ、村松 英、ウェールズ FA、他。mRNA へのプソイドウリジンの組み込みにより、翻訳能力と生物学的安定性が向上した優れた非免疫原性ベクターが得られます [J]。分子療法、2008.3。チョン A 、カリス PR 。リポソーム技術とその全身遺伝子送達への応用における最近の進歩[J]。Advanced Drug Delivery Reviews、1998、30(1-3):73.4。Kulkarni JA、Witzigmann D、Chen S、他。siRNA 治療薬の臨床応用のための脂質ナノ粒子技術[J]。化学研究の会計、2019、52(9).5。カリコ、カタリン、マッデン 他脂質ナノ粒子に含まれてさまざまな経路でマウスに送達されたヌクレオシド修飾 mRNA の発現動態[J]。Journal of Controlled Release 制御放出学会公式ジャーナル、2015.6。単回低用量ヌクレオシド修飾 mRNA ワクチン接種によるジカウイルス防御[J]。ネイチャー、2017、543(7644):248-251.7。パーディ N 、セクレト AJ 、シャン X ら広範囲中和抗体をコードするヌクレオシド修飾 mRNA の投与は、ヒト化マウスを HIV-1 攻撃から保護します [J]。Nature Communications、2017、8:14630.8。Stadler CR、B?Hr-Mahmud H、Celik L、他。mRNAにコードされた二重特異性抗体によるマウスの大きな腫瘍の除去[J]。自然医学、2017.9。NN Zhang、Li XF、Deng YQ 他COVID-19 に対する熱安定性 mRNA ワクチン[J]。セル、2020.10.D Laczkó、Hogan MJ、Toulmin SA、他。ヌクレオシド修飾 mRNA ワクチンによる単回免疫は、マウスの SARS-CoV-2 に対する強力な細胞性および体液性免疫応答を誘発する - ScienceDirect[J]。2020.11.レデラー K 、カスタオ D 、アトリア DG 他SARS-CoV-2 mRNA ワクチンは、中和抗体の生成に関連する強力な抗原特異的胚中心反応を促進します[J]。免疫、2020、53(6):1281-1295.e5.12。Huang Q 、 Ji K 、 Tian S 、 他単回投与の mRNA ワクチンは、hACE2 トランスジェニック マウスを SARS-CoV-2 から長期的に保護します [J]。ネイチャーコミュニケーションズ.13。Vogel AB 、Kanevsky I 、Ye C ら。免疫原性 BNT162b ワクチンは、アカゲザルを SARS-CoV-2 から守ります[J]。自然、2021:1-10。
投稿日時: 2022 年 6 月 20 日