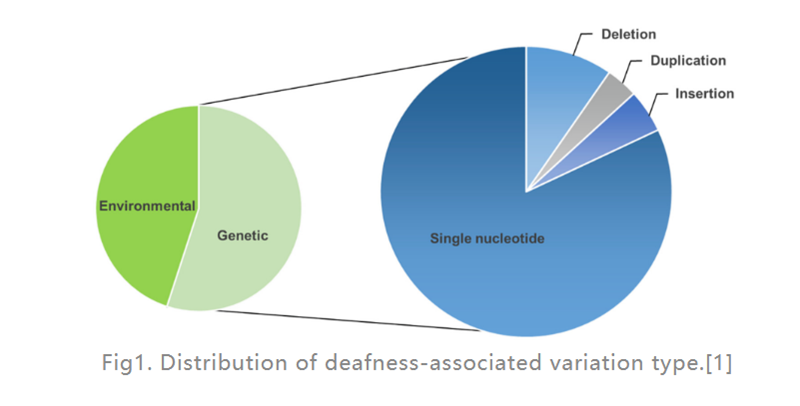
難聴 (HL) は、人間で最も一般的な感覚障害疾患です。先進国では、小児の言語前難聴の約 80% が遺伝的要因によって引き起こされています。最も一般的なのは単一遺伝子の欠陥 (図 1 を参照) で、124 個の遺伝子変異がヒトの非症候性難聴に関連していることが判明しており、残りは環境要因によって引き起こされます。人工内耳 (内耳に設置され、聴神経に直接電気刺激を与える電子機器) は、重度の HL を治療するための最も効果的な選択肢ですが、補聴器 (音波を変換および増幅する外部電子機器) は、中等度の HL の患者を助けることができます。しかし、現在、遺伝性HL(GHL)の治療に利用できる薬剤はありません。近年、遺伝子治療は内耳機能障害を治療するための有望なアプローチとしてますます注目を集めています。
図1.難聴に関連した変動タイプの分布。[1]
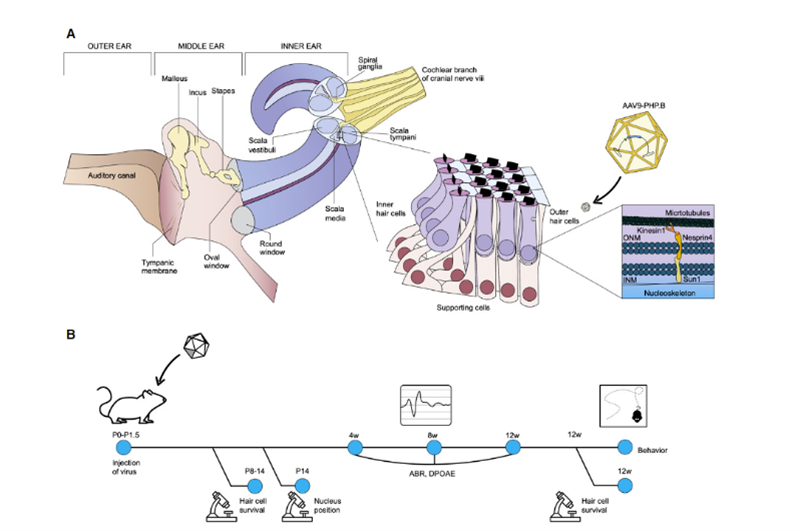
最近、ソーク研究所とシェフィールド大学の科学者らは、分子療法 – 方法と臨床開発 [2] で研究結果を発表し、遺伝性難聴の in vivo 遺伝子治療の広範な応用の見通しを示しました。ソーク研究所の助教授であり、ウェイト先端バイオフォトニクスセンター所長のウリ・マナー氏は、生まれつき重度の難聴を患っており、聴力を回復することは素晴らしい贈り物になると感じていると語った。彼の以前の研究では、Eps8 がアクチン結合およびキャッピング活性を持つアクチン調節タンパク質であることが判明しました。蝸牛有毛細胞では、Eps8 と MYO15A、WHIRLIN、GPSM2、GNAI3 によって形成されるタンパク質複合体が主に長い不動毛の先端に存在し、MYO15A とともに短い不動毛の先端に BAIAP2L2 を局在させ、毛束の維持に必要です。したがって、Eps8 は、正常な聴覚機能に不可欠な有毛細胞の不動毛の長さを調節できます。Eps8 の欠失または変異により不動毛が短くなり、脳の知覚のために音を電気信号に適切に変換できなくなり、難聴につながります。。同時に、共同研究者であるシェフィールド大学教授のウォルター・マルコッティ氏は、Eps8 が存在しないと有毛細胞が正常に発達できないことを発見した。この研究では、マナー氏とマルコッティ氏が協力して、不動毛様細胞に Eps8 を添加することで細胞の機能が回復し、ひいてはマウスの聴力が向上するかどうかを調査しました。研究チームは、アデノ随伴ウイルス (AAV) ベクター Anc80L65 を使用して、正円窓膜注射によって野生型 EPS8 を含むコード配列を Eps8-/- 新生 P1-P2 マウスの蝸牛に送達しました。マウスの蝸牛有毛細胞では、不動毛の機能は成熟する前に修復されました。そして修復効果は画像技術と不動毛の測定によって特徴付けられました。その結果、Eps8 が不動毛の長さを増加させ、低周波細胞の有毛細胞の機能を回復することが示されました。彼らはまた、時間の経過とともに、細胞がこの遺伝子治療によって救出される能力を失うようであることも発見した。Eps8-/-有毛細胞はマウス誕生後に成熟するか、修復不可能なほどの損傷を蓄積している可能性があるため、この治療法は子宮内で投与する必要がある可能性があることが示唆されている。「Eps8 はさまざまな機能を持つタンパク質であり、まだ研究すべきことがたくさんあります」とマナー氏は言う。今後の研究には、さまざまな発達段階での聴覚の回復における Eps8 遺伝子治療の効果の調査や、治療機会を延長できるかどうかの調査が含まれる予定です。偶然にも、2020年11月、イスラエルのテルアビブ大学のKarenB Avraham教授は、革新的な遺伝子治療技術を使用して無害な合成アデノ随伴ウイルスAAV9-PHPを作成した結果をEMBO分子医学誌[3]に発表した。B、Syne4-/-マウスの有毛細胞の遺伝子欠陥は、Syne4のコード配列を運ぶウイルスをマウスの内耳に注射することによって修復され、ウイルスが有毛細胞に侵入し、運ばれている遺伝物質を放出することで、有毛細胞が成熟して正常に機能できるようになった(図2参照)。
図2.コルチ器官とネスプリン 4 の細胞機能に焦点を当てた、内耳の解剖学的構造の概略図。
治療のために変異遺伝子を挿入、除去、または修正する(つまり、病気の遺伝子変化を制御する)ことによって、遺伝子レベルで遺伝性疾患を治療するという目的を達成するための遺伝子治療の使用は、高い臨床効果をもたらすことがわかります。アプリケーションの見通し。遺伝的欠損性難聴に対する現在の遺伝子治療法は、次のカテゴリーに分類できます。
遺伝子置換
遺伝子置換はおそらく、遺伝子治療の最も「単純な」形式であり、欠陥遺伝子を特定し、その遺伝子の正常または野生型コピーと置換することに基づいています。小胞性グルタミン酸トランスポーター 3 (VGLUT3) 遺伝子の欠失によって引き起こされる難聴に対する内耳遺伝子治療研究が初めて成功。内耳有毛細胞(IHC)における外因性 VGLUT3 過剰発現の AAV1 媒介送達は、持続的な聴覚回復、部分的なリボン シナプス形態の回復、およびけいれん反応を引き起こす可能性があります [4]。ただし、上記の序論で説明した2つのAAV送達遺伝子置換を含む例では、特定の種類の遺伝子欠失遺伝性難聴障害に使用されるマウスモデルはヒトとは時間的に異なり、P1マウスでは内耳が発達の成熟段階にあることに注意することが重要です。対照的に、人間は成熟した内耳を持って生まれます。この違いにより、遺伝子治療が成熟したマウスの耳に送達されない限り、マウスの結果をヒトの遺伝性難聴障害の治療に応用することができなくなります。
遺伝子編集: CRISPR/Cas9
「遺伝子の置き換え」に比べ、遺伝子編集技術の発展は、遺伝病を根本から治療する黎明期をもたらしました。重要なことは、遺伝子編集法は、優性遺伝性難聴疾患には適さない従来の過剰発現遺伝子治療法の欠点と、過剰発現法が長く続かないという問題を補うことである。中国の研究者がAAV-SaCas9-KKH-Myo6-g2遺伝子編集システムを使用してMyo6WT/C442YマウスのMyo6C442Y変異対立遺伝子を特異的にノックアウトしたところ、ノックアウトから5か月以内にマウスモデルの聴覚機能が回復した。同時に、内耳の有毛細胞の生存率が向上し、繊毛の形状が規則正しくなり、電気生理学的指標が修正されることも観察されました[5]。これは、Myo6遺伝子変異による遺伝性難聴の治療にCRISPR/Cas9技術を用いた世界初の研究であり、遺伝性難聴の治療における遺伝子編集技術の重要な研究進歩である。治療の臨床翻訳は、確かな科学的根拠を提供します。
遺伝子治療の実施方法
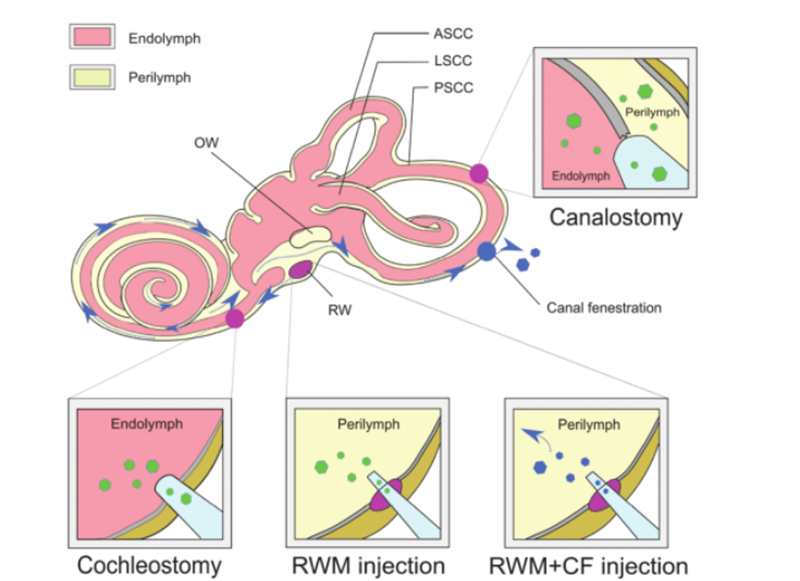
遺伝子治療を成功させるためには、裸の DNA 分子はその親水性とリン酸基の負電荷のため、効果的に細胞に浸透することができません。また、補充された核酸分子の完全性を確保するには、安全で効果的な方法を選択する必要があります。補充された DNA は、標的細胞または組織に送達されます。AAV は、その高い感染効果、低い免疫原性、およびさまざまな組織タイプへの広範な指向性により、疾患治療のための送達媒体として広く使用されています。現在、多くの研究成果により、マウス蝸牛のさまざまな細胞型に対する AAV のさまざまなサブタイプの指向性が決定されています。AAV 送達特性を細胞特異的プロモーターと組み合わせて使用すると、細胞特異的発現を達成でき、オフターゲット効果を低減できます。さらに、従来の AAV ベクターの代替として、新しい合成 AAV ベクターが絶えず開発されており、内耳で優れた伝達能力を示しており、その中で AAV2/Anc80L65 が最も広く使用されています。非ウイルス送達方法は、物理的方法 (マイクロインジェクションおよびエレクトロポレーション) と化学的方法 (脂質ベース、ポリマーベース、および金ナノ粒子) にさらに分類できます。どちらのアプローチも遺伝性難聴障害の治療に使用されており、異なる利点と限界が示されています。ビヒクルとしての遺伝子治療のための送達ビヒクルに加えて、異なる標的細胞タイプ、投与経路、および治療効果に基づいて、インビボ遺伝子投与のための異なるアプローチを使用することができる。内耳の構造が複雑なため、標的細胞に到達するのが難しく、ゲノム編集剤の配布も遅くなります。膜迷路は側頭骨の骨迷路内に位置し、蝸牛管、半円管、卵形嚢、バルーンが含まれます。その相対的な隔離、最小限のリンパ循環、および血液迷路障壁による血液からの分離により、治療薬の効果的な全身送達は新生仔マウスのみに制限されます。遺伝子治療に適したウイルス力価を得るには、内耳にウイルスベクターを直接局所注射する必要があります。確立された注射経路には、(1) 正円窓膜 (RWM)、(2) 気管切開、(3) 内リンパまたは外リンパの蝸牛切開、(4) 正円窓膜とチューブ開窓術 (CF) が含まれます [6] (図 3 参照)。
図3.遺伝子治療の内耳送達。
臨床トランスレーショナル目標に基づいて、遺伝子治療は多くの進歩を遂げてきたが、遺伝子治療が遺伝性疾患患者の第一選択治療選択肢となるには、特に安全で効果的なベクターと送達方法の開発において、さらなる研究が必要である。しかし、近い将来、この種の治療法は個別化療法の定番となり、遺伝性疾患を持つ人々とその家族の生活に大きなプラスの影響を与えると私たちは信じています。
Foregene は、RNA 抽出を行わずに逆転写反応や qPCR 反応を迅速に実行できる、標的遺伝子のハイスループット スクリーニング キットも発売しました。
製品リンク
Cell Direct RT-qPCR キット - Taqman/SYBR GREEN I
製品の詳細については、以下にお問い合わせください。
投稿時間: 2022 年 9 月 2 日