PCR(ポリメラーゼ連鎖反応)は、30年以上の歴史を持つ体外DNA増幅技術の一つです。
PCR 技術は、1983 年に米国シータスの Kary Mullis によって開拓されました。Mullis は 1985 年に PCR 特許を申請し、同年にサイエンス誌に最初の PCR 学術論文を発表しました。マリスはその業績により 1993 年にノーベル化学賞を受賞しました。
PCRの基本原理
PCR はターゲット DNA 断片を 100 万倍以上増幅できます。その原理は、親鎖 DNA を鋳型として、特定のプライマーを伸長の開始点として使用する、DNA ポリメラーゼの触媒作用のもとにあります。これは、変性、アニーリング、伸長などのステップを通じて in vitro で複製されます。親鎖テンプレート DNA に相補的な娘鎖 DNA のプロセス。
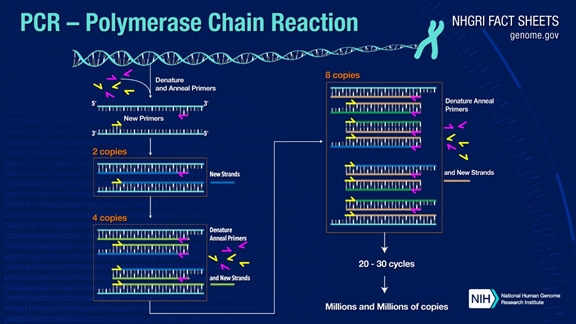
標準的な PCR プロセスは 3 つのステップに分かれています。
1.変性: 高温を使用して DNA 二本鎖を分離します。DNA二本鎖間の水素結合は高温(93~98℃)で切れます。
2.アニーリング:二本鎖DNAを分離した後、プライマーが一本鎖DNAに結合できるように温度を下げます。
3.伸長:温度が下がると、DNAポリメラーゼは結合したプライマーからDNA鎖に沿って相補鎖の合成を開始します。伸長が完了すると一周期が完了し、DNA断片の数が2倍になります。
これら 3 つのステップを 25 ~ 35 回繰り返すと、DNA 断片の数が指数関数的に増加します。
PCR の巧妙な点は、標的遺伝子ごとに異なるプライマーを設計できるため、標的遺伝子断片を短時間で増幅できることです。
これまでのところ、PCR は通常の PCR、蛍光定量 PCR、デジタル PCR の 3 つのカテゴリに分類できます。
通常のPCRの第一世代
通常のPCR増幅装置を用いて目的遺伝子を増幅し、その後アガロースゲル電気泳動を用いて産物を検出するため、定性分析のみが可能です。
第一世代 PCR の主な欠点:
1.非特異的増幅および偽陽性結果が発生しやすい。
2.検出に時間がかかり、操作が煩雑である。
3.定性試験のみ可能
第二世代リアルタイム PCR
リアルタイム PCR は qPCR とも呼ばれ、反応系の進行を示す蛍光プローブを使用し、蛍光シグナルの蓄積により増幅産物の蓄積を監視し、蛍光曲線により結果を判定します。Cq 値と標準曲線を利用して定量化できます。
qPCR 技術は閉鎖系で実行されるため、汚染の可能性が低減され、定量的な検出のために蛍光シグナルを監視できるため、臨床現場で最も広く使用されており、PCR の主流の技術となっています。
リアルタイム蛍光定量 PCR で使用される蛍光物質は、TaqMan 蛍光プローブ、分子ビーコン、蛍光色素に分けられます。
1)TaqMan蛍光プローブ:
PCR 増幅中に、一対のプライマーを追加すると同時に、特定の蛍光プローブが追加されます。プローブはオリゴヌクレオチドであり、両端がレポーター蛍光基とクエンチャー蛍光基で標識されている。
プローブが損傷を受けていない場合、レポーターグループによって発せられる蛍光シグナルは消光グループによって吸収されます。PCR 増幅中、Taq 酵素の 5'-3' エキソヌクレアーゼ活性によりプローブが切断および分解され、レポーター蛍光基とクエンチャーが形成されます。蛍光基は分離されるため、蛍光モニタリング システムは蛍光シグナルを受信できます。つまり、DNA 鎖が増幅されるたびに蛍光分子が形成され、蛍光シグナルの蓄積は PCR 産物の形成と完全に同期します。
2) SYBR蛍光色素:
PCR反応系には過剰のSYBR蛍光色素が添加されます。SYBR 蛍光色素は、DNA 二本鎖に非特異的に組み込まれた後、蛍光シグナルを発します。鎖に組み込まれていない SYBR 色素分子は蛍光シグナルを発しないため、蛍光シグナルが確実に得られます。PCR 産物の増加は PCR 産物の増加と完全に同期します。SYBR は二本鎖 DNA にのみ結合するため、融解曲線を使用して PCR 反応が特異的かどうかを判断できます。
3) 分子ビーコン:
5末端と3末端で約8塩基のヘアピン構造を形成するステムループ二重標識オリゴヌクレオチドプローブです。両端の核酸配列は相補的に対になっており、蛍光基と消光基が緊密になっています。近づけると蛍光は発生しません。
PCR産物が生成された後、アニーリングプロセス中にモレキュラービーコンの中央部分が特定のDNA配列とペアになり、蛍光遺伝子がクエンチャー遺伝子から分離されて蛍光が発生します。
第二世代 PCR の主な欠点:
感度がまだ不足しており、低コピー検体の検出は不正確です。
バックグラウンド値の影響があり、干渉を受けやすい結果となります。
反応系に PCR 阻害剤が存在する場合、検出結果が干渉を受けやすくなります。
第三世代デジタル PCR
デジタル PCR (DigitalPCR、dPCR、Dig-PCR) は、エンドポイント検出を通じてターゲット配列のコピー数を計算し、内部対照や標準曲線を使用せずに正確な絶対定量検出を実行できます。
デジタル PCR はエンドポイント検出を使用し、Ct 値(サイクル閾値)に依存しないため、増幅効率の影響が少なく、PCR 反応阻害剤に対する耐性が向上し、高い精度と再現性が得られます。
高感度・高精度という特徴により、PCR反応阻害剤による干渉を受けにくく、標準品を使用せずに真の絶対定量を実現できるため、研究・応用のホットスポットとなっています。
反応ユニットのさまざまな形式に応じて、マイクロ流体システム、チップシステム、液滴システムの 3 つの主なタイプに分類できます。
1) マイクロ流体デジタル PCR、mdPCR:
マイクロ流体技術に基づいて、DNAテンプレートが分離されます。マイクロ流体技術はサンプルのナノアップグレードやより小さな液滴の生成を実現できますが、液滴は特別な吸着方法を必要とし、その後PCR反応システムと組み合わせる必要があります。mdPCR は徐々に他の方法に取って代わられて採用されています。
2) 液滴ベースのデジタル PCR、ddPCR:
油中水滴生成技術を使用してサンプルを液滴に処理し、核酸分子を含む反応系を数千のナノスケール液滴に分割します。各液滴には検出対象の核酸標的分子が含まれないか、またはテスト対象の1~数個の核酸標的分子が含まれます。
3) チップベースのデジタル PCR、cdPCR:
統合流体経路技術を使用して、シリコンウェーハまたは石英ガラス上に多数のマイクロチューブとマイクロキャビティを彫刻し、さまざまな制御バルブを介して溶液の流れを制御し、デジタル PCR 反応用の反応ウェルにサンプル液体を同じサイズのナノメートルに分割して絶対定量を達成します。
第 3 世代 PCR の主な欠点:
装置や試薬は高価です。
テンプレートの品質要件は高いです。鋳型量がマイクロシステム量を超えると定量できなくなり、少なすぎると定量精度が低下します。
非特異的な増幅がある場合にも、偽陽性が発生する可能性があります。
投稿時間: 2021 年 7 月 30 日